Đề thi thử THPTQG môn Hóa - THPT Đoàn Thượng năm 2015
26/03/2015 17:40 pm
Đề thi thử THPT quốc gia môn Hóa trường THPT Đoàn Thượng - Hải Dương năm 2015, các em tham khảo dưới đây:
|
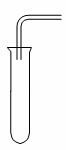
Đề thi thử THPTQG môn Hóa THPT Đoàn Thượng năm 2015 - Mã đề 132 Cho nguyên tử khối của một số nguyên tố: H=1, He=4, C=12, N=14, O=16, Li=7, Na=23, Mg=24, Al=27, S=32, Cl=35,5, K=39, Ca=40, Fe=56, Cu=64, Zn=65, Br=80, Ag=108, Ba=137. Câu 1: Tripanmitin có công thức là A. (C17H31COO)3C3H5. B. (C17H35COO)3C3H5. C. (C15H31COO)3C3H5. D. (C17H33COO)3C3H5. Câu 2: Đốt Fe trong khí clo thiếu thu được hỗn hợp X gồm 2 chất rắn. Hai chất trong X là A. FeCl3 và Fe. B. FeCl2 và Fe. C. FeCl2 và FeCl3. D. FeO và FeCl2. Câu 3: Hoà tan hoàn toàn hỗn hợp gồm 0,01 mol FeS2 và y mol Cu2S vào axit HNO3 (vừa đủ), thu được ddX (chỉ chứa hai muối sunfat) và V lít khí NO2 (đkc, sản phẩm khử duy nhất). Giá trị của V là A. 2,912. B. 2,24. C. 4,48. D. 3,136. Câu 4: Cho các chất sau: glucozơ, axetilen, saccarozơ, anđehit axetic, but-2-in, etyl fomat. Số chất khi tác dụng với dung dịch AgNO3 (NH3, to) cho kết tủa là A. 3. B. 2. C. 5. D. 4. Câu 5: X là một este no, đơn chức, mạch hở. Trong phân tử X có ba nguyên tử cacbon. Số CTCT của X thoả mãn là A. 3. B. 4. C. 2. D. 5. Câu 6: Điện phân có màng ngăn với điện cực trơ 400 ml dung dịch hỗn hợp gồm CuSO4 xM và NaCl 1M với cường độ dòng điện 5A trong 3860 giây. Sau khi ngừng điện phân thấy khối lượng dung dịch tạo thành bị giảm so với ban đầu là 10,4 gam. Giá trị của x là A. 0,2. B. 0,1. C. 0,129. D. 0,125. Câu 7: Cho Mg vào dung dịch chứa FeSO4 và CuSO4. Sau phản ứng thu được chất rắn A chỉ có một kim loại và dung dịch B chứa 2 muối. Phát biểu nào sau đây đúng? A. FeSO4 dư, CuSO4 chưa phản ứng, Mg hết. B. CuSO4 dư, FeSO4 chưa phản ứng, Mg hết. C. CuSO4 hết, FeSO4 chưa phản ứng, Mg hết. D. CuSO4 và FeSO4 hết, Mg dư. Câu 8: Đun nóng m gam hỗn hợp X (R-COO-R1; R-COO-R2) với 500 ml dung dịch NaOH 1,38M thu được dung dịch Y và 15,4 gam hỗn hợp T gồm hai ancol đơn chức là đồng đẳng liên tiếp. Cho toàn bộ lượng T tác dụng với Na dư thu được 5,04 lít khí hiđro (đktc). Cô cạn Y thu được chất rắn rồi lấy chất rắn này đem nung với CaO xúc tác đến khi phản ứng xảy ra hoàn toàn thu được 7,2 gam một khí. Giá trị của m là A. 20,44. B. 40,60. C. 34,51. D. 31,00. Câu 9: Chất nào sau đây là amin no, đơn chứa, mạch hở? A. CH3N. B. CH4N. C. CH5N. D. C2H5N. Câu 10: Cho từ từ 200 gam dung dịch NaOH 8% vào 150 gam dung dịch AlCl3 10,68% thu được kết tủa và dung dịch X. Cho thêm m gam dung dịch HCl 18,25% vào dung dịch X thu được 1,17 gam kết tủa và dung dịch Y. Nồng độ % của NaCl trong dung dịch Y là A. 5,608% hoặc 6,830%. B. 6,403% hoặc 6,830%. C. 6,403% hoặc 8,645%. D. 5,608% hoặc 8,645%. Câu 11: Trong công nghiệp, natri hiđroxit được sản xuất bằng phương pháp A. Điện phân dung dịch NaCl, không có màng ngăn điện cực. B. Điện phân dung dịch NaCl, điện cực trơ, có màng ngăn điện cực. C. Điện phân dung dịch NaNO3, không có màng ngăn điện cực. D. Cho dung dịch Ba(OH)2 tác dụng với xođa (Na2CO3). Câu 12: Hoà tan hết 17,724 gam hỗn hợp Al và Mg trong dung dịch HNO3 loãng, dư thu được dung dịch X (chứa ba chất tan) và 6,272 lít hỗn hợp khí Y không màu (chỉ gồm hai chất, một chất bị hoá nâu trong không khí) có khối lượng 10,36 gam. Biết thể tích khí đo ở đkc. Số mol HNO3 đã phản ứng và tổng khối lượng muối (gam) thu được khi cô cạn dung dịch X lần lượt là A. 1,96 và 113,204. B. 0,56 và 43,764. C. 1,4 và 87,164. D. 1,86 và 104,524. Câu 13: Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và Al2O3 nung nóng đến khi phản ứng hoàn toàn, thu được8,3 gam hỗn hợp chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là A. 0,8 gam. B. 2,0 gam. C. 8,3 gam. D. 4,0 gam. Câu 14: Cho hình vẽ thu khí như sau:
Những khí nào trong số các khí H2, N2, NH3 ,O2, Cl2, CO2, HCl, SO2, H2S có thể thu được theo cách trên? A. H2, NH3, N2, HCl, CO2. B. H2, N2, NH3, CO2. C. O2, Cl2, H2S, SO2, CO2, HCl. D. Tất cả các khí trên. Câu 15: Hỗn hợp X gồm CH3OH, C2H5OH, C3H7OH và H2O. Cho m gam X tác dụng với Na dư thu được 0,7 mol H2. Đốt cháy hoàn toàn m gam X thu được 2,6 mol H2O. Giá trị của m là A. 24. B. 42. C. 36. D. 32. Câu 16: Cho anđehit X tác dụng với lượng dư dung dịch AgNO3 trong NH3 (to) thu được muối Y. Biết muối Y vừa có phản ứng tạo khí với dung dịch NaOH, vừa có phản ứng tạo khí với dung dịch HCl. Công thức của X là A. CH3CHO. B. HCHO. C. (CHO)2. D. CH2=CH-CHO. Câu 17: X là este tạo từ axit đơn chức và ancol đa chức. X không tác dụng với Na. Thủy phân hoàn toàn a gam X cần dùng vừa đủ 100 gam dung dịch NaOH 6% thu được 10,2 gam muối và 4,6 gam ancol. Vậy công thức của X là A. (HCOO)2C2H4. B. (C2H3COO)3C3H5. C. (CH3COO)2C3H6. D. (HCOO)3C3H5. Câu 18: Hợp chất hữu cơ X có công thức phân tử trùng với công thức đơn giản nhất chứa C, H, O, N. Đốt cháy hoàn toàn 10,8 gam X thu được 4,48 lít CO2, 7,2 gam H2O và 2,24 lít khí N2 (khí đo ở đkc). Nếu cho 0,1 mol chất X trên tác dụng với dung dịch chứa 0,2 mol NaOH đun nóng thu được chất khí làm xanh giấy quỳ tím ẩm và dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan. Giá trị của m là A. 15. B. 21,8. C. 5,7. D. 12,5. Câu 19: Cho hỗn hợp X gồm 0,1 mol C2H4 và 0,1 mol CH4 qua 100 gam dung dịch Br2 thấy thoát ra hỗn hợp khí Y có tỷ khối so với H2 là 9,2. Vậy nồng độ % của dung dịch Br2 là A. 12%. B. 14%. C. 10%. D. 8%. Câu 20: Nhận xét nào sau đây đúng? A. CaSO4.2H2O dùng để bó bột khi gãy xương. B. Cho Zn nguyên chất vào dung dịch HCl thì có ăn mòn điện hoá. C. CaCO3 tan trong H2O có CO2. D. Khi đun nóng thì làm mềm nước cứng vĩnh cửu. Câu 21: Hỗn hợp X gồm hiđro, propen, propanal, ancol alylic (CH2=CH-CH2OH). Đốt cháy hoàn toàn 1 mol hỗn hợp X thu được 40,32 lít CO2 (đkc). Đun X với bột Ni, sau một thời gian thu được hỗn hợp Y, tỉ khối hơi của Y so với X là 1,25. Dẫn 0,1 mol hỗn hợp Y qua dung dịch brom dư, thấy hết m gam brom. Giá trị của m là A. 8,0. B. 16,0. C. 4,0. D. 12,0. Câu 22: Dãy gồm tất các các chất không phản ứng với HNO3 đặc nguội là A. Al, Fe, Cr, Cu. B. Fe2O3, Fe, Cu. C. Fe, Cr, Al, Au. D. Fe, Al, NaAlO2. Câu 23: Polime poli(vinyl clorua) là sản phẩm trùng hợp của monome nào sau đây? A. CN-CH=CH2. B. CH2=CH2. C. C6H5-CH=CH2. D. CH2=CH-Cl. Câu 24: Dung dịch NaOH phản ứng được với tất cả các chất trong dãy nào sau đây? A. CuSO4; FeO; HCl. B. Ba; phenol; MgO. C. HNO3; FeCl2; Al(OH)3. D. Al2(SO4)3; Al; NaAlO2. Câu 25: Hai nguyên tố X, Y thuộc cùng nhóm và ở hai chu kỳ liên tiếp nhau có tổng số số hiệu nguyên tử là 32. Vậy X, Y thuộc nhóm nào? A. VIIA. B. IIIA. C. VIA. D. IIA. Câu 26: Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (đkc). Khối lượng dung dịch thu được sau phản ứng là A. 101,48 gam. B. 101,68 gam. C. 88,20 gam. D. 97,80 gam. Câu 27: Hoà tan hết 17,92 gam hỗn hợp X gồm Fe3O4, FeO, Fe, CuO, Cu, Al và Al2O3 (trong đó Oxi chiếm 25,446% về khối lượng) vào dung dịch HNO3 loãng dư, kết thúc các phản ứng thu được dung dịch Y và 1,736 lít (đkc) hỗn hợp khí Z gồm N2 và N2O, tỉ khối của Z so với H2 là 15,29. Cho dung dịch NaOH tới dư vào Y rồi đun nóng, không có khí thoát ra. Số mol HNO3 đã phản ứng với X là A. 0,75. B. 1,392. C. 1,215. D. 1,475. Câu 28: X là tetrapeptit Ala-Gly-Val-Ala, Y là tripeptit Val-Gly-Val. Đun nóng m gam hỗn hợp X và Y có tỉ lệ số mol nX : nY = 1 : 3 với 780 ml dung dịch NaOH 1M (vừa đủ), sau khi phản ứng kết thúc thu được dung dịch Z. Cô cạn dung dịch Z thu được 94,98 gam muối. m có giá trị là A. 68,10 gam. B. 64,86 gam. C. 77,04 gam. D. 65,13 gam Câu 29: Hãy cho biết loại polime nào sau đây có cấu trúc mạch phân nhánh? A. cao su lưu hóa. B. poli (metyl metacrylat). C. xenlulozơ. D. amilopectin. Câu 30: Hấp thụ hết V lít CO2 (đkc) bởi dung dịch có chứa 0,08 mol Ca(OH)2 ta thu được 2 gam kết tủa, lọc kết tủa, thu lấy phần nước lọc, khối lượng của phần nước lọc tăng so với khối lượng dung dịch Ca(OH)2 ban đầ 4,16 gam. Giá trị của V là A. 3,136. B. 4,480. C. 3,360. D. 0,448. Câu 31: Kim loại nào sau đây không tan trong dung dịch NaOH dư? A. Na. B. Fe. C. Ba. D. Al. Câu 32: Cho các chất Cu, Fe, Ag và các dung dịch HCl, CuSO4, FeCl2, FeCl3. Số cặp chất có phản ứng với nhau là A. 4. B. 5. C. 2. D. 3. Câu 33: Đốt cháy hoàn toàn 10,0 gam chất hữu cơ X có công thức phân tử là C5H8O2 bằng oxi. Sau đó cho toàn bộ sản phẩm cháy vào 2,0 lít dung dịch Ca(OH)2 thu được 10,0 gam kết tủa. Nồng độ mol/l của dung dịch Ca(OH)2 là A. 0,30 M. B. 0,15 M. C. 0,20 M. D. 0,25 M. Câu 34: Cho sơ đồ phản ứng sau: NaOH → X1 → X2 → X3 → NaOH. Vậy X1, X2, X3 lần lượt là A. Na2CO3, NaHCO3 và NaCl. B. NaCl, Na2CO3 và Na2SO4. C. Na2SO4, NaCl và NaNO3. D. Na2SO4, Na2CO3 và NaCl Câu 35: Nhận xét nào sau đây không đúng? A. Al2O3 là hợp chất lưỡng tính. B. Tất cả các kim loại nhóm IIA đều phản ứng với H2O ở điều kiện thường. C. Trong hợp chất Al chỉ có số oxi hoá +3. D. Tất cả các kim loại nhóm IA đều phản ứng với H2O ở điều kiện thường. Câu 36: Nguyên tử X có cấu hình electron ở lớp ngoài cùng là 3s1. Trong hai nguyên tử X có tổng số hạt mang điện là A. 22. B. 21. C. 44. D. 42. Câu 37: Cho các chất sau: xenlulozơ, amilozơ, amilopectin, glicogen, mantozơ và saccarozơ. Số chất có cùng công thức (C6H10O5)n là A. 5. B. 6. C. 3. D. 4. Câu 38: Dãy gồm các chất đều có khả năng làm đổi màu dung dịch quì tím ẩm là A. CH3NH2, C6H5OH, HCOOH. B. C6H5NH2, C2H5NH2, HCOOH. C. CH3NH2, C2H5NH2, H2N-CH2-COOH. D. CH3NH2, C2H5NH2, HCOOH. Câu 39: Dung dịch axit acrylic (CH2=CH-COOH) không phản ứng được với chất nào sau đây? A. Cu(OH)2. B. MgCl2. C. Br2. D. Na2CO3. Câu 40: Trường hợp nào dưới đây hỗn hợp chất rắn không bị hòa tan hết (giả thiết các phản ứng xảy ra hoàn toàn)? A. Cho hỗn hợp chứa 0,10 mol Cu và 0,10 mol Ag vào dung dịch HNO3 đặc, nóng chứa 0,5 mol HNO3. B. Cho hỗn hợp chứa 0,10 mol Mg và 0,10 mol Zn vào dung dịch chứa 0,5 mol HCl. C. Cho hỗn hợp chứa 0,05 mol Ba và 0,10 mol Al vào nước dư. D. Cho hỗn hợp chứa 0,10 mol Fe2O3 và 0,10 mol Cu vào dung dịch HCl dư. Câu 41: So sánh tính chất của glucozơ, tinh bột, saccarozơ, xenlulozơ. (1) Cả 4 chất đều dễ tan trong nước và đều có các nhóm -OH. (2) Trừ xenlulozơ, còn lại glucozơ, tinh bột, saccarozơ đều có thể tham gia phản ứng tráng bạc. (3) Cả 4 chất đều bị thủy phân trong môi trường axit. (4) Khi đốt cháy hoàn toàn 4 chất trên đều thu được số mol CO2 và H2O bằng nhau. (5) Cả 4 chất đều là các chất rắn, màu trắng. Trong các so sánh trên, số so sánh không đúng là A. 4. B. 5. C. 2. D. 3. Câu 42: Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hoà của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Số muối của kim loại M thoả mãn là A. 2. B. 0. C. 3. D. 1. Câu 43: Cho các phản ứng sau: (1) BaCO3 + dung dịch H2SO4; (2) dung dịch Na2CO3 + dung dịch FeCl2; (3) dung dịch Na2CO3 + dung dịch CaCl2; (4) dung dịch NaHCO3 + dung dịch Ba(OH)2; (5) dung dịch (NH4)2SO4 + dung dịch Ba(OH)2; (6) dung dịch Na2S + dung dịch CuSO4. Số phản ứng tạo đồng thời cả kết tủa và khí bay ra là A. 2. B. 5. C. 4. D. 3. Câu 44: Chất nào sau đây là etylamin? A. C2H7N. B. C2H3NH2. C. CH3NH2. D. C2H5NH2. Câu 45: Chất nào sau đây là este? A. CH3OOCC2H5. B. HOOCCH3. C. C2H5Cl. D. (CH3CO)2O. Câu 46: Khi thủy phân hoàn toàn 90,6 gam một tetrapeptit (tạo từ alanin) bằng dung dịch NaOH vừa đủ thì khối lượng muối thu được là A. 133,2 gam. B. 106,8 gam. C. 444 gam. D. 126,6 gam. Câu 47: Phát biểu nào sau đây không đúng? A. Chỉ số axit là số mg KOH để trung hoà axit béo tự do có trong 1 gam chất béo. B. Thuỷ phân hoàn toàn tinh bột (H+, to) thu được glucozơ. C. Oxi hoá glucozơ bằng H2 (Ni, to) thu được sobitol. D. Dùng nước Br2 để chứng minh ảnh hưởng của nhóm -NH2 đến nhóm -C6H5 trong phân tử anilin. Câu 48: Cho 3 chất hữu cơ X, Y, Z (mạch thẳng, chỉ chứa C, H, O) đều có khối lượng mol là 82 (trong đó X và Y là đồng phân của nhau). Biết 1,0 mol X hoặc Z tác dụng vừa đủ với 3,0 mol AgNO3 trong dung dịch NH3; 1,0 mol Y tác dụng vừa đủ với 4,0 mol AgNO3 trong dung dịch NH3. Kết luận không đúng khi nhận xét về X, Y, Z là A. Số liên kết π trong X, Y và Z lần lượt là 4, 4 và 3. B. Phần trăm khối lượng của hiđro trong X là 7,32% và trong Z là 2,44%. C. Phần trăm khối lượng oxi trong X là 39,02% và trong Z là 19,51%. D. Số nhóm chức -CHO trong X, Y và Z lần lượt là 1,2 và 1. Câu 49: Nguyên tắc luyện thép từ gang là A. Dùng CaO hoặc CaCO3 để khử tạp chất Si, P, S, Mn,… trong gang để thu được thép. B. Dùng O2 oxi hoá các tạp chất Si, P, S, Mn,… trong gang để thu được thép. C. Dùng chất khử CO khử oxit sắt thành sắt ở nhiệt độ cao. D. Tăng thêm hàm lượng cacbon trong gang để thu được thép. Câu 50: Hãy cho biết yếu tố nào sau đây luôn không làm chuyển dịch cân bằng hoá học? A. Nồng độ B. Áp suất C. Xúc tác. D. Nhiệt độ. Đáp án sẽ được Tuyensinh247 cập nhật sau, các em chú ý theo dõi. Nguồn: Dethi.violet 🔥 2K9 CHÚ Ý! LUYỆN THI TN THPT - ĐÁNH GIÁ NĂNG LỰC - ĐÁNH GIÁ TƯ DUY!
️🎯 LỘ TRÌNH SUN 2027 - LUYỆN THI TN THPT - ĐGNL - ĐGTD (3IN1)
|
>> Đề thi thử THPT quốc gia môn Hóa - THPT Cẩm Giàng II năm 2015
>> Đề thi thử THPT Quốc gia môn Toán THPT Cẩm Bình 2015
Viết bình luận: Đề thi thử THPTQG môn Hóa - THPT Đoàn Thượng năm 2015
- Đề thi thử môn Văn tốt nghiệp THPT 2026 - Cụm chuyên môn 12 Đắk Lắk (lần 2) (19/05/2026)
- Đề thi thử vào lớp 10 chuyên 2026 môn Toán - THCS Cầu Giấy (lần 1) (19/05/2026)
- Đề thi thử tốt nghiệp THPT 2026 môn Hóa - Sở GD Vĩnh Long (19/05/2026)
- Đề thi thử môn Địa tốt nghiệp THPT 2026 - Sở GD Lâm Đồng (19/05/2026)
Tin tức mới nhất
- Thời gian nộp hồ sơ đăng ký xét tuyển các trường Đại học 2026
- Thông tin tuyển sinh Đại học Công thương TPHCM 2026
- Thông tin tuyển sinh Viện nghiên cứu và đào tạo Việt Anh - ĐH Đà Nẵng 2026
- Thông tin tuyển sinh ĐH Khoa học và Công nghệ Hà Nội năm 2026
- Thông tin tuyển sinh trường Đại học Kỹ thuật - Công nghệ Cần Thơ năm 2026
- Hơn 1.500 học sinh TP HCM được tuyển thẳng vào lớp 10